
製品説明
| 次亜リン酸基本情報 |
| 概要 化学的性質 用途 毒性 危険有害性の特定 製造方法 製造方法 |
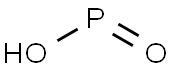
| 製品名: | 次亜リン酸 |
| 同義語: | 次亜リン酸、30%(W/V)溶液;次亜リン酸、50%(W/V)溶液;次亜リン酸:(ホスフィン酸);次亜リン酸、50% w/w 水溶液;次亜リン;次亜リン酸(腐食性液体、酸性、無機、無);次亜リン酸、50%w/waq.溶液;次亜リン酸溶液 50% 水溶液 |
| CAS:の | 6303-21-5 |
| MF: | HO2Pの |
| MW:の | 63.980501 |
| EINECS: | 228-601-5 |
| 製品カテゴリー: | HPA;無機物;6303-21-5 |
| Mol ファイル: | 6303-21-5.モル |
 |
|
| 次亜リン酸の化学的性質 |
| 融点 | -25度 |
| 沸点 | 108度(759.8513 mmHg) |
| 密度 | 20度で1.206 g/mL(リットル) |
| 蒸気圧 | <17 mmHg ( 20 °C) |
| 保管温度 | 制限はありません。 |
| 溶解度 | H2O、エタノール、エチルエーテルに非常に溶けやすい |
| ピーカ | pK1 1.1。 |
| 形状 | 吸湿性の結晶または無色の油状液体 |
| 色 | 無色 |
| 水溶性 | 可溶性 |
| メルク | 13,4894 |
| 安定性: | 安定。強塩基とは互換性がありません。酸化剤、強塩基、硝酸水銀(II)、酸化水銀(II)と激しく反応します。100℃以上に加熱しないでください。 |
| InChIKey(インチャイキー) | GQZXNSPRSGFJLY-UHFFFAOYSA-N |
| CAS データベースリファレンス | 6303-21-5(CAS データベース リファレンス) |
| NIST化学リファレンス | 次亜リン酸(6303-21-5) |
| EPA 物質登録システム | ホスフィン酸(6303-21-5) |
| 安全情報 |
| 危険コード | C |
| リスクステートメント | 34 |
| 安全に関する声明 | 26-36/37/39-45 |
| リダドル | 国連 3264 8/PG 3 |
| WGKドイツ | 1 |
| RTECS について | SZ6400000 |
| TSCAの | はい |
| 危険クラス | 8 |
| 梱包グループ | Ⅱ |
| HSコード | 28111990 |
| 有害物質データ | 6303-21-5(有害物質データ) |
| MSDS情報 |
| プロバイダー | 言語 |
|---|---|
| ホスフィン酸 | 英語 |
| シグマアルドリッチ | 英語 |
| アクロス | 英語 |
| アルファ | 英語 |
| 次亜リン酸の使用と合成 |
| 概要 | 次亜リン酸は「次亜リン酸塩」とも呼ばれ、無色の油または潮解性結晶で、重要なファインケミカル製品です。主な用途は無電解メッキの還元剤、リン樹脂の変色防止、エステル化反応触媒、冷媒、特に高純度製品次亜リン酸ナトリウムの製造に使用できます。製造方法はいくつかありますが、一般的な工業的製造方法はイオン交換樹脂法と電気透析法です。 次亜リン酸の化学的性質、用途、毒性、製造方法は、Chemicalbook の andy によって編集されています。(2016-12-04) |
| 化学的性質 | 潮解性の結晶または無色の油です。融点は26.5度です。比重は1.439(固体、19度)。水、エタノール、エーテルに溶け、水、エタノール、アセトンと任意の割合で混合できます。空気中では容易に潮解してシロップ状の液体になり、水溶液は酸性です。 次亜リン酸は一塩基酸で、水溶液では強酸で、Ka=10-2 (25 度 ) です。室温では比較的安定しています。130 度で不均化反応が進行し、ホスフィンと亜リン酸に分解します。 2H3PO2=H3PO4+PH3 強力な還元力があり、重金属塩溶液はCu2 +、Hg2 +、Ag +などの金属に戻すことができます。 4Ag+H3PO2+2H2)=4Ag+H3PO4+4H+ 弱い酸化剤ですが、強い還元剤と接触するとホスフィンに還元されます。 |
| 用途 | 1. 次亜リン酸は無電解メッキの還元剤として使用されます。 2.リン酸樹脂の変色防止に使用できます。 3.エステル化触媒、冷媒として使用されます。 4. 次亜リン酸塩、ナトリウム塩、マンガン塩、鉄塩の製造に使用され、一般的に栄養物質として使用されます。 5. 次亜リン酸は、医療分野で還元剤として、またヒ素やテルルの測定、タンタルやニオブなどの試薬の分離に使用されます。 6. 強力な還元剤であり、次亜リン酸ナトリウム、リン酸カルシウム、その他の次亜リン酸の製造に使用できます。 7. メッキ浴、医薬品、還元剤、一般試薬などに使用できます。 8. 強力な還元剤であり、次亜リン酸ナトリウム、リン酸カルシウム、その他の次亜リン酸の製造に使用できます。 9. この製品は還元剤として広く使用されており、Ag、Cu、Ni、Hgなどの金属を対応する金属に還元し、As、Nb、Taなどの試薬の検証に使用したり、Na、K、Ca、Mn、Feなどのタイプの次亜リン酸塩の製造に使用したりできます。 |
| 毒性 | 不燃性ですが、正孔水素化剤と接触すると火災の原因になります。酸化剤と接触すると、激しい反応と燃焼が進行する可能性があります。高温になると、非常に有毒なホスフィンガスに分解したり、爆発したりする可能性があります。腐食性があります。次亜リン酸は、吸収されないため、ソフトドリンクによく添加されます。そのため、リスクは小さいですが、特に強い次亜リン酸は胃腸を傷つけます。誤って目に入ったり、皮膚に接触した場合は、大量の水で洗い流してください。製造作業者は保護服などの保護具を着用する必要があります。製造設備は密閉し、作業場は十分に換気する必要があります。 |
| 危険物の特定 | 危険情報: 重度の皮膚の火傷や目の損傷を引き起こします。 重篤な眼障害を引き起こす 注意事項: 粉塵/煙/ガス/ミスト/蒸気/スプレーを吸入しないでください。 取り扱い後はよく洗ってください。 保護手袋と目/顔の保護具を着用してください。 飲み込んだ場合: 口をすすいでください。無理に吐かせないでください。 皮膚(または髪)に付着した場合:直ちに汚染された衣類をすべて脱いでください。皮膚を水またはシャワーで洗い流してください。 目に入った場合:数分間水で注意深く洗い流してください。 簡単にできます。すすぎを続けます。 吸入した場合: 被害者を新鮮な空気のある場所に移し、呼吸しやすい姿勢で休息させてください。 直ちに中毒センターまたは医師に連絡してください。 施錠して保管してください。 この物質とその容器を危険物または特別廃棄物収集場所に廃棄してください。 |
| 調理方法 | 1. リンと水酸化バリウムの溶液を加熱すると、バリウム塩 Ba (H2PO2) 2・2H2O が生成され、硫酸を次亜リン酸バリウム溶液に加えると、Ba2+ が沈殿します。 Ba(H2PO2)2+H2SO4=BaSO4+2H3PO2 次亜リン酸は、減圧蒸発と低温結晶化によって得られます。このプロセスではバリウム塩の溶解度が低いため、得られる次亜リン酸の濃度は高くなく、工業製品は再結晶化によって精製する必要があります。 2. 酸化バリウム(または石灰)と白リンの溶液を加熱して二次リン酸バリウム(またはカルシウム)を形成し、硫酸と反応させて濾過、濃縮して生成物を得るか、または次亜リン酸ナトリウム溶液をH型イオン交換樹脂に通して生成物を得ることができます。この方法は大量の樹脂を必要とし、樹脂の再生と洗浄のステップが面倒で、一般的に1ポンドあたり7ドル以上のコストがかかり、小規模バッチ生産にのみ適しており、大規模な工業用途には適していません。 3. 次亜リン酸は電気透析法で製造され、電気透析セルは陽極室、原料室、陰極室の3つの部分に分かれ、中間層は陰イオン膜と陽イオン膜で分離され、2つの膜の間に次亜リン酸ナトリウム溶液(濃度100g/L〜500g/L)が置かれ、陽極室は次亜リン酸の希薄溶液5g/L、陽極室は希薄水酸化ナトリウム溶液(5g /L)であり、極間に直流(3V〜36V)が通され、陽極は酸素を放出し、次亜リン酸の二次生成物を生成します。陰極は水素を放出し、水酸化ナトリウムの二次生成物を生成します。反応時間は3〜21時間です。陽極室と陰極室の反応は次のとおりです。 陽極室: H2O==H++OH- 2OH-==O2+2H2O+4e H++H2PO2-==H3PO2 陰極室: H2O==H++OH- 2H++2e==H2 Na++OH-==NaOH 次亜リン酸は電気透析法で製造方法が簡単で設備投資も少なく、大量生産に適しています。 4. 工業用グレードの次亜リン酸ナトリウムから始めて、次亜リン酸の品質指標に影響を与えるCl-、SO42-アニオンを沈殿によって除去し、硫化物を形成することによって溶液から重金属イオンを除去し、次に強酸性陽イオン交換樹脂を使用して第二リン酸ナトリウムを得ることで、高純度グレードの製品を得ることができます。 このプロセスは高品質の第二リン酸を生産することができ、技術的に実現可能であり、プロセスはシンプルで操作が簡単で、製品品質が良好であり、電子産業、防衛産業、その他のハイテク分野のニーズを満たすことができます。 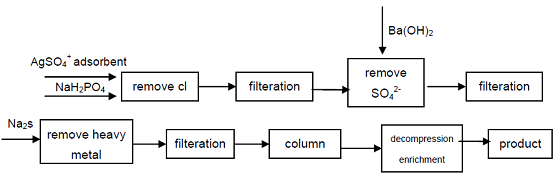 図1 工業用次亜リン酸ナトリウムから次亜リン酸を製造するプロセス。 5. イオン交換樹脂法:水で湿らせた陽イオン交換樹脂約70gをガラス管に詰め、5mol/L塩酸を約15分間循環させ、水で十分に洗浄した後、高純度次亜リン酸ナトリウム水溶液(15g/60ml H2O)を流し、樹脂カラムを最初に50mlで洗浄し、次に25mlの蒸留水で洗浄します。流出酸と洗浄液を合わせ、水浴で蒸発させて濃縮します。濃縮した酸をP205乾燥機で高真空に置き、脱水、冷却、結晶化、濾過、再結晶化して次亜リン酸製品を得ます。 |
| 製造方法 | イオン交換樹脂法:水溶性陽イオン交換樹脂約70gをガラス管に入れ、5mol/L塩酸で約15分間循環させ、水で十分に洗浄します。高濃度次亜リン酸ナトリウム水溶液(15g/60ml H2O)を樹脂カラムに流し、最初に50mlの水で洗浄し、次に25mlの蒸留水ですすぎます。流出酸と洗浄液を合わせ、水浴で蒸発させて濃縮します。濃縮酸を高真空P205乾燥機に送って脱水し、冷却結晶化、濾過、再結晶化を行って次亜リン酸の完成品を得ます。 |
| 説明 | 次亜リン酸は、分子式 H3PO2 の強力な還元剤です。無機化学者は、この遊離酸をこの名前で呼んでいますが、IUPAC 名はジヒドリドヒドロオキシドオキシドリン、またはホスフィン酸の許容名です。次亜リン酸は、水、ジオキサン、アルコールに溶ける無色の低融点化合物です。次亜リン酸の式は一般に H3PO2 と表記されますが、より説明的な表記は HOP(O)H2 で、これは一価の特質を強調しています。この酸から得られる塩は、ホスフィン酸塩 (次亜リン酸塩) と呼ばれます。 |
| 説明 | この酸は、一般式 H4P2O6 を持ち、他のオキシ亜リン酸とは異なります。多くの特殊性があります。リンが湿った空気によって酸化されると、亜リン酸およびリン酸とともに生成されます。白リンを空気にさらし、生成した液体に酢酸ナトリウムを加えると、やや不溶性の次亜リン酸ナトリウム Na2H2P2O6·6H2O が分離します。しかし、次亜リン酸ナトリウム一水和物は、-98.7 g/100 ml で非常に溶解性が高く、潮解性があります。 |
| 化学的性質 | 無色の液体 |
| 物理的特性 | 無色の潮解性結晶または油状液体。酸っぱい臭い。密度 1.493 g/cm3。融点 26.5 度。沸騰点 130 度。水、アルコール、エーテルに非常に溶けやすい。50% 水溶液の密度は 1.13 g/mL。 |
| 用途 | 次亜リン酸は、主に無電解ニッケルめっきに使用されます。アレーンジアゾニウム塩の還元に関与します。フィッシャーエステル化反応の添加剤として機能します。また、中和剤、酸化防止剤、重合および重縮合の触媒、湿潤剤としても機能します。さらに、医薬品の配合、ポリマーの脱色、水処理、貴金属または非鉄金属の回収にも使用されます。これに加えて、プラスチック、合成繊維の漂白剤、脱色剤、および化学薬品やさまざまなプラスチックの製造中の色安定化剤として使用されます。 |
| 準備 | 次亜リン酸はさまざまな方法で製造できます。 1. 白リンを水酸化カルシウムで煮沸する: P4+ 4Ca(OH)2 + 8H2O → 4Ca(H2PO2)2 + 4H2 カルシウム塩は水に溶けます。硫酸で処理すると次亜リン酸が生成されます。 (H2発注書2)2Ca + H2それで4 → 2H3発注書2+ CaSO4 生成物の混合物を濾過して不溶性のCaSO4を除去する。次亜リン酸水溶液を減圧下で濃縮する。水酸化カルシウムの代わりに濃縮バリタ水を使用することもできる。2.次亜リン酸ナトリウムNaH2PO2をイオン交換樹脂で処理する。ナトリウム塩は、白リンを水酸化ナトリウム溶液で沸騰させることによって生成することができ、これは上記(1)と同様の反応である。 フィリピン3 + 2I2 + 2H2O → H3発注書2+ 4こんにちは 上記の方法は、白リンをアルカリで加熱する方法よりも安全であると考えられます。 次亜リン酸は50度以下で保管する必要があります。市販されているものは様々な濃度の水溶液です。 |
| 生産方法 | 次亜リン酸は、次亜リン酸バリウムと硫酸を反応させ、硫酸バリウムを濾過することによって生成されます。溶液を真空中で 80 度で蒸発させ、その後 0 度に冷却すると、次亜リン酸が結晶化します。 |
| 意味 | ChEBI: 単一の五価リンが単結合を介して 2 つの水素とヒドロキシ基に、また二重結合を介して酸素に共有結合したリンオキソ酸。ホスフィン酸のクラスの親。 |
| 意味 | 白色の結晶性固体。一塩基酸で、陰イオンHを形成する。2発注書2– 水中。黄リンを水酸化ナトリウム溶液で加熱することで、ナトリウム塩、つまり酸を生成できます。遊離酸とその塩は強力な還元剤です。 |
| 反応 | 次亜リン酸は、あらゆる割合で水と混和し、市販の濃度は 30% H3PO2 です。次亜リン酸塩は医療に使用されます。次亜リン酸は強力な還元剤で、例えば硫酸銅と反応すると、水素化銅 Cu2H2 という茶色の沈殿物が形成され、温めると水素ガスを発生して銅が残ります。硝酸銀と反応すると、細かく砕かれた銀が生成されます。亜硫酸と反応すると、硫黄と少量の硫化水素が生成されます。硫酸と反応すると亜硫酸が生成され、これは上記と同様に反応し、過マンガン酸塩と反応すると直ちにマンガンを形成します。 |
| 概要 | 次亜リン酸は、酸っぱい臭いのある無色の油状液体または潮解性結晶として現れます。密度は 1.439 g / cm3 です。融点は 26.5 度です。蒸気を吸入すると、呼吸器官が刺激されたり、火傷を負ったりします。液体および蒸気は、目や皮膚を刺激したり、火傷を負ったりすることがあります。 |
| 空気と水の反応 | 潮解性。水溶性。 |
| 反応性プロファイル | 次亜リン酸は加熱するとリン酸と自然発火性のホスフィンに分解します。硫酸によって酸化され、二酸化硫黄と硫黄を放出します。酸化水銀(II)と爆発的に反応します[Mellor, 1940, Vol. 4, 778]。硝酸水銀(II)と激しく反応します[Mellor, 1940, Vol. 4, 993]。発熱反応で塩基を中和します。 |
| 危険 | 酸化剤と接触すると火災や爆発の危険があります。 |
| 健康被害 | 有毒。物質を吸入、摂取、または皮膚に接触すると、重傷または死亡の原因となる場合があります。溶融物質に接触すると、皮膚や目に重度の火傷を負う可能性があります。皮膚との接触は避けてください。接触または吸入の影響は遅れて現れる場合があります。火災により、刺激性、腐食性、および/または有毒なガスが発生する可能性があります。消火剤または希釈水からの流出水は、腐食性および/または有毒で、汚染を引き起こす可能性があります。 |
| 火災の危険性 | 不燃性。物質自体は燃えませんが、加熱すると分解して腐食性および/または有毒な煙を発生することがあります。一部は酸化剤であり、可燃物(木材、紙、油、衣類など)に引火する可能性があります。金属と接触すると可燃性の水素ガスが発生する場合があります。容器は加熱すると爆発する可能性があります。 |
| 精製方法 | リン酸は、市販の 50% 次亜リン酸の一般的な汚染物質です。Jenkins と Jones [J Am Chem Soc 74 1353 1952] は、1 L フラスコ内の約 600 mL を 40 度で減圧 (N2 中) し、約 300 mL の容量まで蒸発させることでこの物質を精製しました。溶液を冷却した後、広口の三角フラスコに移し、ストッパーで密閉し、ドライアイス/アセトン浴に数時間放置して凍結させました (必要に応じて、壁をこすりました)。フラスコを約 5 度で 12 時間放置すると、約 30-40% が液化したので、再度濾過しました。このプロセスを繰り返し、固体を真空デシケーター内の Mg(ClO4)2 上で冷蔵保存しました。その後、室温で溶解し、氷塩浴で-20oで冷却してn-ブタノールから結晶化させたが、それ以上精製されなかった。遊離酸はm 26.5oで潮解性結晶を形成し、H2OおよびEtOHに溶解する。NaH2PO2塩は、陰イオン交換樹脂で精製できる[Klement Z Anorg Allgem Chem 260 267 1949.] |
| 次亜リン酸製剤および原材料 |
| 原材料 | アンバーライト(R) IRC-50 |
| 準備製品 | XANTHURENIC ACID-->3,5-diisopropylphenol-->cmtirust agent T-708-->Sodium hypophosphite-->TRIS(2,2'-BIPYRIDYL)RUTHENIUM(II) CHLORIDE HEXAHYDRATE-->4-IODOPYRIDINE-2-CARBOXYLIC ACID-->2,3,5,6-Tetrafluorophenol-->Benzothiazole, 4-methyl- (7CI,8CI,9CI)-->BEHENIC ACID METHYL ESTER-->リン酸 |
人気ラベル: 次亜リン酸、中国の次亜リン酸メーカー、サプライヤー、工場
あなたはおそらくそれも好きでしょう
お問い合わせを送る



